Elementi di metallurgia
Diagrammi di "Solvus"
descrivono il comportamento delle sostanze
- pure,
- miscugli.
Durante i passaggi di stato, indicano
- le fasi,
- la composizione e
- la quantità.
Definizioni:
- Sistema: porzione di materia in esame;
- Fase: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite;
- Sostanza pura: porzione di materia con un solo componente chimico;
- Miscuglio: porzione di materia costituito da due o più sostanze pure.
Trasformazione dell'acqua in funzione della temperatura e della pressione
(considerazioni con l'aumento della temperatura)
A pressione atmosferica, il ghiaccio si trasformerà in acqua a 0°C, per poi trasformarsi in vapore saturo a 100°C;
- ad una pressione inferiore all'atmosferica, l'acqua, sotto forma di ghiaccio, si scioglierà un poco al di sopra dello 0°C, mentre si trasformerà in vapore a pressione inferiore a 100°C. Nel campo navale si sfrutta questa caratteristica per aumentare il rendimento della produzione di acqua distillata. Uno o più eiettori provvedono a ridurre la pressione negli "evaporatori" o "distillatori":
- a pressione superiore all'atmosferica, il ghiaccio si scioglierà a temperature leggermente inferiori allo 0°C, mentre l'ebollizione avverrà a temperature sopra a 100°C.Nel campo industriale e navale si sfrutta questa caratteristica per aumentare il rendimento della produzione del vapore nelle caldaie.
NOTA FOLCLORISTICA: La pastasciutta che si mangia in montagna è sempre "scotta"; infatti, data la minor pressione atmosferica dovuta all'altezza del monte (Stevino), l'acqua bolle prima di raggiungere i 100°C ...
Diagrammi TTT dell'acqua a pressione ambiente
Trasformazione Temperatura Tempo.
L'acqua è una sostanza "pura".
Durante i passaggi di stato la temperatura si mantiene costante.
Nel passaggio da uno stato inferiore ad uno superiore sarà necessario somministrare l'energia sotto forma di calore.
1) Sosta termica 100°C
2) sosta termica 0°C
3) calore sensibile
4) calore latente
5) stato solido
6) solido-liquido
7) stato liquido
8) liquido-aeriforme
9) aeriforme
Sostanza pura
Comportamento del piombo puro al variare della temperatura
Diagramma TTT di un miscuglio
Il miscuglio non percorre il cambiamento di stato come le sostanze pure.
La soluzione solidifica a temperatura più bassa (curva a tratti)
Diagrammi di equilibrio
in rosso le regioni monofasiche
in giallo le regioni bifasiche
L regione liquida bifasica
Completa miscibilità allo stato solido (Cu-Ni) lega omogenea
La fusione del miscuglio, avrà luogo entro valori di temperature sino ad una temperatura limite in cui tutto il solido sarà fuso.
Dall'alto verso il basso: Inizio della solidificazione del componente con temperatura di fusione più alta
Reticolo CFC cubico a facce centrate (1).

1) Solido,
2) lliquido,
3) liquido e fase alto fondente,
4) Curva solidus, al di sotto di essa, tutto è solido,
5) curva liquidus, al di sopra di essa tuto è liquido,
6) Cu, basso fondente,
7) Ni, alto fondente.
I cristalli che si formano nello stato solido hanno dimensioni pressocché uguale, da cui consegue il concetto di di LEGA OMOGENEA.

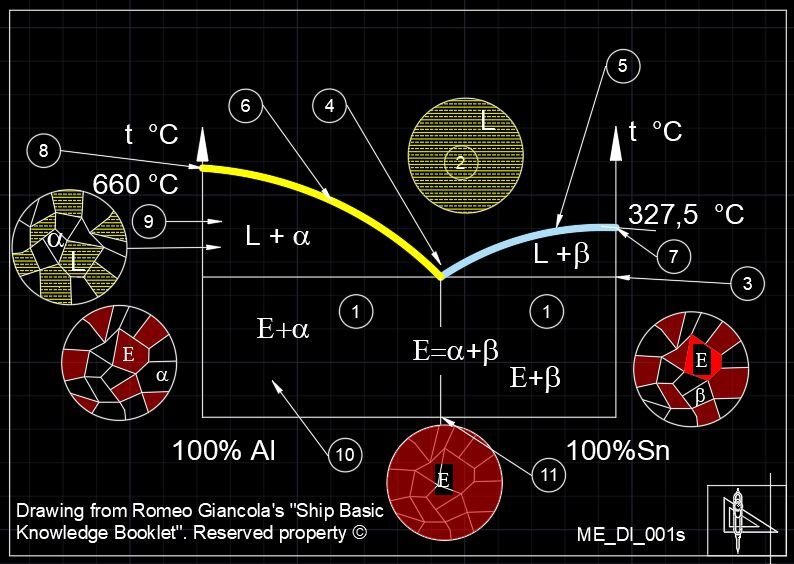
Completa immiscibilità allo stato solido (Al-Sn), leghe eterogenee
Lega eterogenea
Caratterizzata dal punto triplice "E", eutettico, cui i due metalli fondono alla temperatura più bassa e vi è una triplice presenza di fasi liquide. Raffreddando lentamente si otterrà la lega eutettica.
Sotto l'orizzontale di eutettico si avranno, a sinistra della verticale della lega di eutettico, cristalli di eutettico e cristalli di alluminio; a destra cristalli di eutettico cristalli di stagno.
1) Solido,
2) liquido,
3) orizzontale di eutetico,
4) punto di EUTETICO,
5) curva liquidus Sn,
6) Curva liquidus Al,
7) temperatura di fusione del Sn,
8)Temperatura di fusione di Al.ì,
9) Compresenza della fase Al che si è solidificata per prima e di fase liquida,
10) al passaggio della linea di eutectico, tutta la fase liquida si solidifica, ma la fase precedentemente solidificata prevale nelle dimensioni, rispetto alla fase che solidifica per ultima,
11) l'Eutectico ha cristalli dei due elementi pressocché di eguali dimensioni.
Allo stato solido i cristalli di Al sono più grandi dei cristalli di Eutettico, analogamente i cristalli di beta sono più grandi dei cristalli dell'Eutectico. per questa ragione si chiama lega eterogenea.
Queste leghe hanno resistenza meccanica inferiore alla lega di Eutectico che ha cristalli dei due componenti di eguali dimensioni, ovvero cristalli omogenei.
Miscibilità parziale allo stato solido (Pb-Sn)
Questo diagramma comprende i due precedenti ed aggiunge la fase solida monofase sia di Pb che di Sn

La soluzione solidifica a temperatura più
bassa (curva tratti)
___
Diagramma ferro carbonio
Di fatto è un diagramma ferro cementite: Fe- Fe3C (tre atomi di ferro ed un atomo di carbonio).
Fe3C carburo di ferro è un composto metastabile, ovvero l'atomo di carbonio tende a separarsi da Fe3, con formazione di Fe3 e grafite, ma in un tempo estremamente lungo.

Contenuto di carbonio degli acciai:
- C <0,77% acciaio ipoeutettoide,
- C = 0.77% acciaio eutettoide,
- 0,77%< C < 2,06% acciaio ipereuttoide,
- C> 2,11% ghisa
Punti notevoli del diagramma di stato Fe-C
Sono quelli che presentano tre fasi contemporaneamente (punti tripli)
- Punto eutectoide “S”, 0,77% di C e 727°C;
- Punto eutecttico “C”, 4,30% di C e 1147°C;
- Punto peritettico “J” 0,17% di C e 1493°C.
L’ aumento della percentuale di carbonio nella lega causa:
- aumento di resistenza a, compressione, durezza, fusibilità,
- diminuzione di resilienza, allungamento, saldabilità, fucinabilità.
(Resilienza: energia che può essere assorbita nel campo delle deformazioni plastiche).
Ferro α
Ferrite (Fe alfa) curva di solvus GPQ.
Reticolo Cubico a Corpo Centrato (CCC)
Sino 911°C (entro triangolo QPG)
770°C temperatura di Curie
Il reticolo Cubico a Corpo Centrato è composto da due atomi (a sinistra);
Il reticolo Cubico a Facce Centrate, proprio del ferro γ è composto da quattroatomi (a destra).




Reticolo cubico a facce centrate

Reticolo cubico a corpo centrato

Austenite (Fe γ), Cubico Facce Centrate, Sino 1394°C ferro γ, delimitata dalla curva di solvus-: JN, GS, SE e dalla curva di solidus EJ
Ferro δ
Cubico Corpo Centrato
Sino a 1538°C
Ferro δ
linee di solidus HA e di solvus HN
Temperatura di fusione Fe puro1538°C, 0,0%C

